Stále častěji volíme nejen efektivní, ale současně i ekonomicky výhodné technologie pro zajištění úpravy a čištění vod. Snaha o alternativní, méně chemické a prostředí zatěžující technologie, opětovné využívání šedých vod či nedostatek kvalitní pitné vody jsou pro budoucnost zcela zásadní a klíčové. Perspektivní a ve své podstatě ekologicky šetrnější jsou technologie využívající nanočástice (nanomateriály apod.), které byly úspěšně aplikovány v mnoha odvětvích průmyslu.
Increasingly, we choose not only efficient but also cost effective technology for water treatment. The pursuit of alternative, less stressful environment and chemical technologies, reuse of gray water or the lack of quality drinking water is vital for the future of a key. Perspective and inherently more environmentally friendly technologies are utilizing nanoparticles (nano-materials, etc.) that have been successfully applied in many industries. Effectiveness of the application of nanoparticles (metals) technology for many years studied and verified in practice, therefore offering their application in water treatment technology and waste water treatment. This article deals with the possibilities of nanotechnology in water supply, compares the impact of silver nanoparticles on ecosystems algae.
Úvod
Antimikrobiální účinky stříbra jsou známé již od starověku. Oficiálně se koloidní stříbro začalo využívat v medicíně, v době ještě před objevením antibiotik, např. v Evropě a USA v letech 1933 až 1939 při akné, ekzémech, popáleninách, při výskytu kožní plísně a oparu (i pásového), u artrózy, při revmatismu, u zápalu plic, při chřipce atd. Léčebný účinek stříbra je zřejmý, ale přes to není stále možné koloidní stříbro deklarovat jako lék. Například pro celou EU platí, že se nemůže deklarovat pro vnitřní použití, pro zajímavost v České Republice není koloidní stříbro povoleno jako potravinový doplněk. Nanočástice stříbra se začaly aplikovat i do výplňového materiálu používaného v dentální medicíně s prokazatelně významnými antimikrobiálními účinky, ale vzhledem k toxickým účinkům stříbra a nedostatku informací o jeho působení v živých systémech nebylo jeho používání dosud schváleno (García-Contreras 2011).
Stříbro má toxické účinky na většinu mikroorganismů. Ionty stříbra generují uvnitř mikroorganismů volné radikály, které ničí buněčné funkce. Vlivem elektrostatické přitažlivosti je kladně nabitý náboj iontu přitahován k záporně nabitému povrchu buněčné membrány (Kim 2007). U různých druhů organismů byla pozorována indukce oxidativního stresu, a také toxické působení na fotosystém II (probíhá v chloroplastech, nezbytný pro zisk elektronů má redukci oxidu uhličitého na sacharidy). Buňky vystavené oxidativnímu stresu mají poškozené proteiny, nižší mastné kyseliny i DNA, zvýšený podíl peroxidových mastných kyselin, což vede k nezvratnému poškození až ke smrti (Oukarroum 2012, Křížková 2009).
Stříbro se, zejména pro své dezinfekční účinky, velmi často využívá v různých odvětvích průmyslu. Toxických vlastností stříbra se používá významně při likvidace mikrobiální kontaminace (Escherichia coli, Staphylococcus aureus, Pseudomonas aeruginosa, Salmonella sp., Vibrio sp. apod.). Možnosti aplikací na eliminaci dalších organismů, např. sinic, řas, mechorostů a vyšších organismů, se postupně zvažují.
S nástupem nanotechnologií se začalo uvažovat o možném zvýšení toxického účinku stříbra tím, že se připraví nanočástice tohoto kovu. V porovnání s běžně velkými částicemi vykazují nanočástice specifické fyzikální a chemické vlastnosti. Kovové nanočástice inhibují svým toxickým působením buněčný růst, fotosyntetickou i respirační aktivitu (Zhuang Wang 2012). Toxický účinek závisí na koncentraci nanočástic a velmi úzce souvisí s polopropustností buněčné membrány. Působením nanočástic stříbra může dojít ke vzniku nepravidelných pórů ve vnější membráně a tím ke změně její propustnosti, způsobené uvolňováním lipopolysacharidových molekul a membránových proteinů (Kim 2007). Stříbrné nanočástice vyvolávají silný pokles fotosyntézy, což se projevuje na celkovém kvantovém výtěžku primárního fotosystému a na elektronovém transportu (Oukarroum 2012).
Pokud jde o samotný toxický účinek, je zde další otázkou, zda jsou za toxické působení zodpovědné samotné nanočástice, nebo se jedná o toxický efekt iontového stříbra, uvolněného z nanočástice. Dosavadní studie se shodují na faktu, že nelze přičítat toxické působení pouze iontům stříbra, ale i nanočásticím. Účinky se liší u různých typů organismů, rozdílnost v toxickém působení je často vysvětlována na základě trofie (Navarro 2008, Wood 1999). Například pro jednoznačné určení mechanismu toxického působení kovových nanočástic na řasy není dostatek údajů. Většina studií, zabývajících se toxickým působením nanočástic na řasy, ať už mořských (Thalassiosira weissflogii) či sladkovodních (Chlamydomonas reinhardtii a Pseudokirchneriella subcapitata), uvádí, že toxicita byla způsobena právě Ag+ ionty uvolněnými při kontaktu s buňkou (Miao 2010, Navarro 2008, Griffitt 2008, Griffitt2009). Toxický účinek byl, mimo jiné, zjištěn i při testech na perloočkách Ceriodaphnia dubia, nebo na embryích ryb Pimephales promelas (Griffitt 2008, Laban 2010).
Úprava a dezinfekce pitné vody
Zásadním řešeným problémem současné doby je světový nedostatek pitné vody. Nedostatek pitné vody je problém zejména v rozvojových zemích, kde je potřeba zajistit efektivní a ekonomicky výhodnou technologii, pro zajištění úpravy vody. Zejména v oblasti rozvojových zemí, jsou ve vodě stále přítomny patogenní organismy, které je těžké odstranit. Současné chemické technologie dezinfekce vody jsou poměrně nákladné, pokud jde o kapitál, provozní náklady a údržbu objektů. Globální hrozba nedostatku pitné vody a touha po dosažení ekologicky šetrnějších technologiích, dokazuje perspektivní využití nanotechnologií i v oblasti čištění a úpravy vody.
Na počátku 20. století se stříbro využívalo jako antibakteriální vodní filtr (“Katadyn silver”) (Pradeep 2009). Nanočásticemi stříbra se začaly povrchově upravovat různé materiály, např. zeolity, písek vlákna, iontoměniče, aktivní uhlí. Filtrační materiály povrchově potažené nanočásticemi stříbra byly s úspěchem použity na odstranění patogenních bakterií (E. coli, S. typhimurium, S. dysenteriae, V. cholerae) z podzemní vody (Mpenyana-Monyatsi 2012). Nanočásticemi stříbra se začaly potahovat granule aktivního uhlí a následně používat pro dezinfekci vody v Abu Rawash oblasti v Egyptě. Aktivní uhlí se používá jako vysoce účinný sorbent pro odstranění široké škály organismů a anorganického znečištění z vody nebo ze vzduchu. Technologie aplikace nanočástic stříbra výrazně pomohla s eliminací bakterií Escherichia coli v pitné vodě (El – Aassar 2013). V USA se vyvíjí technologie vhodného ukotvení nanočástice stříbra v pórech keramických filtrů, které se používají pro čištění užitkové vody (Ren 2013).
Perspektivní se jeví solární dezinfekce vody využívající nanočástice stříbra a TiO2. Při solární dezinfekci je voda vystavena slunečnímu záření. Dezinfekční účinek zajišťuje UV oblast spektra soustředěná okolo hodnoty 340 nm. Z tohoto důvodu se solární dezinfekce dá využít pouze v oblastech s velkým množstvím sluneční energie, tedy také pro rozvojové země. Hlavním principem metody je fotokatalýza, při které dochází k interakci mezi lehkými a polovodičovými částicemi, které jsou schopné produkovat vysoce oxidativní sloučeniny. Tyto sloučeniny likvidují bakterie a odstraňují značné množství chemických nečistot ve vodě. Nanočástice se využívají jako fotokatalytické polovodiče, nejčastěji v praxi aplikované nanočástice jsou TiO2 (vynikající fotokatalytická aktivita), dále pak ZnO, Fe2O3, WO3 a CdSe. Pro zvýšení účinnosti TiO2 se přidává kovové stříbro. Systém spojení nanočástic TiO2 a stříbra ukazují na lepší inhibiční účinky s minimálním počtem mikroorganismů, než samotné TiO2 (Kumar 2009), zvýšený účinek se projevil nejen na vystavených bakteriích, ale dokonce i virových částicích (Liga 2011).
Antimikrobiální aktivita byla pozorována také ve tmě, což naznačuje zejména účinky stříbra. Výhodou, oproti chemickým metodám, je vyšší rychlost a tedy minimální doba dezinfekce, z toho plynou nižší náklady na údržbu i pořizovací cenu. Vzhledem, k tomu, že při katalýze vznikají poměrně přirozené látky, snižuje se také tvorba nebezpečných látek (Kumar 2009).
Nevýhodou tohoto systému může být použití nanočástic kovů, které je nutné z vody následně odseparovat. Není zcela jisté, jak reagují v lidském těle a v prostředí. Jsou proto omezeny různými zákony a vyhláškami. V pitné vodě nemohou být přítomny. Ovšem jedná se o výhodnou alternativu oproti chemickým metodám, vhodnou také pro rozvojové země, jelikož se jedná o jednoduché a snadno využitelné procesy (Kumar 2009).
Vliv nanočástic při čištění odpadních vod
Nanotechnologie nabízí možnost účinného odstranění mikrobiálního a chemického znečištění z odpadních vod. Jedná se o nanočástice kovů, kterými se potahují různé materiály, zeolity, dendrimery, uhlíkaté materiály. Uhlíkové nanotrubky a nanovlákna vykazují pozitivní výsledky. Účinek nanočástic se umocňuje kombinací více technologií a postupů. Například prostředí s koliformními bakteriemi, které bylo na krátkou dobu vystavené ošetření ultrazvukem se po následné aplikaci nanočástic stříbra zvýšil antibakteriální účinek. Nanočástice stříbra lze využít, na rozdíl od normálního stříbra, pro odstraňování pesticidů. Do budoucna je jistě při čištění odpadních vod dobrou volbou kombinace více technologií (Tiwari 2008, Pradeep 2009).
Nanočástice jsou vynikající adsorbenty, protože mají specifické vlastnosti (velikost, velký reakční povrch, vysoký počet míst pro interakci). Nejčastěji se pro odstraňování polutantů z vody využívá nanočástic oxidu hliníku, železa a titanu. (Ali 2012, Pradeep 2009).
Na čistírnu odpadních vod se kanalizací dostávají průmyslově vyrobené nanočástice. Jedná se zejména o nanočástice používané hlavně v domácnostech, ve zdravotnictví a v potravinářských zařízení. Existuje zde pravděpodobnost usazení nanočástic stříbra v aktivovaném kalu, ale také jejich vyplavení do recipientu. Pokud se dostanou až na čistírnu odpadních vod, jsou většinou ukládány do biomasy a tím jsou odstraněny z odpadní vody, ale na biomasu mohou mít inhibiční účinky. V aktivační části čistírny se ukládají do biomasy. Na biosorpci nanočástic mají vliv nejen vlastnosti odpadní vody, ale svou roli také hrají mikroorganismy, které jsou obsažené v aktivovaném kalu. Nanočástice mají vliv na komplexní mikrobiální společenstvo. Toto působení ovlivňuje fyzická struktura a prostorová distribuce vloček aktivovaného kalu. Vločky aktivovaného kalu jsou složeny z mikroorganismů a extracelulárních biopolymerů, které chrání vločku (Muñoz 2012, Sun 2013, Kaegi 2011).
Vzhledem k inhibičním účinkům, nanočástic na aktivovaný kal je žádoucí, aby se na čistírny odpadních vod dostalo co nejmenší množství nanočástic. Na ukládání a zpracování nanočástic má vliv hned několik faktorů. Nanočástice jsou termodynamicky nestabilní v oxickém prostředí a jsou oxidovány na jiné sloučeniny, například AgCl. Vliv má také speciace nanočástic na přítoku v různých stupních čištění. Dříve byl nejčastější thiolát stříbrný z fotografického průmyslu. Proto v prostředí s dostatečným množstvím anorganických sulfidů a organických ligandů thiolových skupin jsou nanočástice, převážně stříbra, transformovány. Přes všechny studie nejsou dosud zcela známy všechny okolnosti chování nanočástic v odpadní vodě na čistírnách odpadních vod. Vliv má také koncentrace nanočástic (Muñoz 2012, Sun 2013, Kaegi 2011).
Ošetření povrchů nanočásticemi
Nanočástice se začínají postupně aplikovat i ve stavebnictví, do hmot, nátěrů a tmelů, při ochraně povrchů staveb (budov, konstrukcí). Uvažuje se přímá aplikace nanočástic i na památky, které jsou výrazně kontaminovány mikroorganismy (deteriogeny, biodeteriorace). Pojem biodeteriorace zahrnuje nežádoucí změny na povrchu materiálu, ke kterým dochází vlivem činnosti mikroorganismů. Mikroorganismy si pro svou ochranu vytváří biofilm (nahromadění buněk, extracelulární polymerní substance a vody). Stejná problematika se řeší na objektech úpraven vod, vodojemů a čistíren odpadních vod. Jako první kolonizují povrch staveb fototrofní mikroorganismy, které jsou podkladem pro vývoj dalších chemolitotrofních organismů (Adámková 2012).
Experimentální část
Testování řas v roztoku
Pro testování nanočástic stříbra byl zvolen klasický test inhibice růstu sladkovodních řas, který byl na základě ISO 8692 modifikován. Modifikace spočívá ve volbě jiného typu zřeďovací vody (Knoppův roztok), zvýšení výchozí koncentrace řasového inokula (80 tisíc cenobií) a zvolení menšího objemu testovaného roztoku (25 ml). Pro zabránění případné reakci preparátu se zřeďovacím mediem i případné interferenci složek v roztoku byl zvolen jako zřeďovací roztok Knoppův roztok. Tento typ zřeďovací vody obsahuje v předepsaném poměru sloučeniny KNO3, K2HPO4, MgSO4.7H2O a FeCl3. V průběhu testu byla pozorována za použití vhodného fluorescenčního nástavce také vitalita buněk, na základě autofluorescence chlorofylu. Pro doplnění výsledků, vypovídajících o stimulaci či inhibici bylo využito stanovení koncentrace chlorofylu-a (dle ČSN ISO 10 260).
Test inhibice růstu sladkovodních řas probíhá po dobu 96 hodin. Každý den se prošetřuje vzorek testované látky na rastru počítací komůrky (typ Cyrus I), spočítá se počet buněk v 1 ml. Ze zjištěných hodnot počtu cenobií řas se zjistí inhibice růstové rychlosti, či případná hodnota EC50. Jako modelový organismus byla zvolena chlorokokální řasa Desmodesmus quadricauda, kmen Greifswald 15 ze sbírky řas BÚ AVČR Třeboň. Řasa Desmodesmus quadricauda tvoří cenobia o počtu 2 až 8 buněk, netvoří odpočinková stádia a je jednoduchá na kultivaci v laboratorních podmínkách. V přírodě se vyskytuje velmi často.
Chlorokokální řasy nejsou jedinými fototrofními zástupci, které je možné na površích konstrukcí identifikovat. Součástí habitatu povrchů jsou např. vláknité řasy vytvářející masivní povlaky rigidní povahy. Z dostupných zdrojů literatury zabývající se biodeteriorací byly vybrány nejčastěji se vyskytující vláknité řasy např. Klebsormidium sp., Spirogyra lacustris, Ulothrix ef. tenerima a Stigeoclonium sp. Taxony zmíněných řas byly získány ze sbírky řas a použity pro další sadu testů toxicity. Vláknité řasy jsou diskutabilní zkušební organismy, protože není snadné provedení zkoušky toxicity. U organismu není jednoznačná kvantifikace (stélka x buňka) a způsob aplikace inokula ke vzorku. I přes tuto skutečnost je žádoucí testy s těmito organismy uskutečnit a tím rozšířit účinky nanočástic stříbra na tento typ organismu. Řešením, které se nabízí, je založení testu na stanovení koncentrace chlorofylu-a a její případná inhibice či stimulace pro test toxicity.
Testování účinků stříbra na plochách
Veškeré testy toxicity jsou založené na metodě aviatických testů. Principem je příprava vodného výluhu, nadávkování toxické látky a živného roztoku ve vhodném poměru a následné vyhodnocení ukazatelů toxicity. Současná metodika testů toxicity (ISO 8692) vyžaduje používání modelových organismů, kterými jsou sladkovodní chlorokokální řasy. Výsledky z tohoto uspořádání testu nelze adekvátně použít na případné hodnocení vlivu látky na substráty a povrchy porostlé organismy, biofilmy, nárosty apod. Aby bylo možné zodpovědně říci, že přípravek je účinný dávkováním do roztoku také na povrchy, je zásadní vytvořit metodiku pro testování ploch. Vývoj metodiky spočívá především v modifikaci postupu, jenž využívá suspenzi řas zachycenou na filtrech, aplikovaných přímo na živnou půdu. Vyhodnocení testu probíhá makroskopicky (fotografická dokumentace filtrů) počítačovým zpracováním snímků a stanovením inhibice, resp. stimulace, koncentrace chlorofylu-a.
Příprava nanočástic stříbra
Pro testování inhibice růstu sladkovodních řas byly připraveny nanočástice stříbra pomocí Tollensovy metody, při které dochází k redukci stříbrné soli pomocí borohydridu. Takto lze získat nanočástice kovů o velmi malých rozměrech. Metoda přípravy nanočástic byla modifikována pro dosažení ekologicky šetrného roztoku, který by obsahoval pouze nanočástice příslušného kovu. K redukci se proto využívají sacharidy, v tomto případě byly využity monosacharidy glukóza, galaktóza a disacharidy maltóza a laktóza (Panáček 2006).
2 AgNO3 + 2 NaBH4 → 2 Ag0 + 2 NaNO3 + B2H6 +H2 (1)
2 AgNO3 + 2 NH3 + 2 NaBH4 → 2 Ag0 + 2 NaNO3 + B2H6 + H2 + 2 NH3 (2)
Metodou byly získány nanočástice o různé velikosti. Velikost nanočástic v připravených koloidech se pohybovala v rozmezí od 5 nm do 70 nm (viz Tab. 1).
Tab. 1 Velikosti nanočástic jednotlivých přípravků
|
Vzorek č. |
B1 |
B2 |
Gl1 |
M1 |
L1 |
G1 |
|
Ag [nm] |
5 |
9 |
20 |
37 |
43 |
70 |
(Komentář: přípravu nanočástic zajistilo pracoviště Ústavu fyzikální chemie J. Heyrovského AV ČR, v.v.i. Praha)
Výsledky akvatických testů
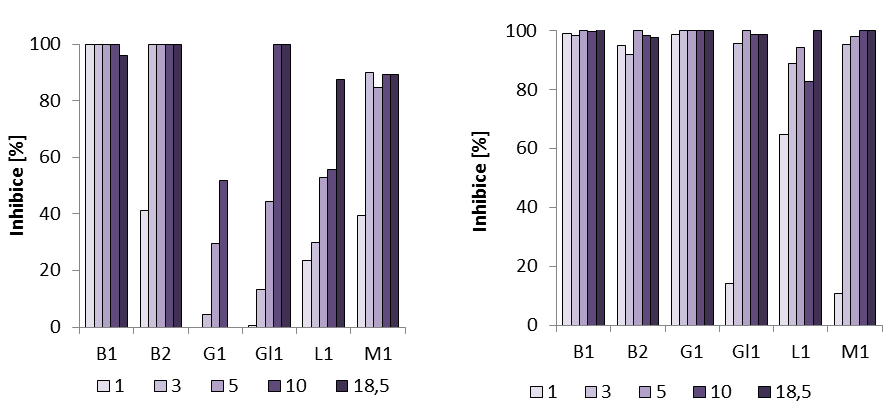
Přípravek B1, byl vysoce účinný, a to pro všechny druhy otestovaných řas. 100% inhibice se projevila již při koncentraci 1ppm a to hned po 24 hodinách expozice (viz Obr. 2). U přípravků připravených redukcí cukrem, G1 a Gl1 docházelo během testu u řasy Desmodesmus quadricauda k shlukování cenobií, což bylo pravděpodobně způsobeno ochrannými mechanismy, vytváření obalů a využívání cukrů. Při testování těchto preparátů na vláknité řasy se projevila 100% inhibice u koncentrací vyšších než 1ppm. Z cukerných koloidů se jako nejúčinnější jevil, pro chlorokokální řasu Desmodesmus quadricauda maltózový koloid M1, v případě vláknitých řas byl nejúčinnější galaktózový koloid G1.
Při mikroskopické analýze byly pozorovány četné tmavé shluky na povrchu řasových cenóbií, které jsou opatřeny sporopoleninovou vrstvou. Pravděpodobně na této pevné konstrukci (obalu buňky) se kumulují částice kovu, které brání řase v jejím metabolismu. I když může být stínící efekt sporný, je velice pravděpodobné, že za větší míru mortality buněk mohl právě popsaný efekt „navazování/nabalování“ stříbra na buňky.
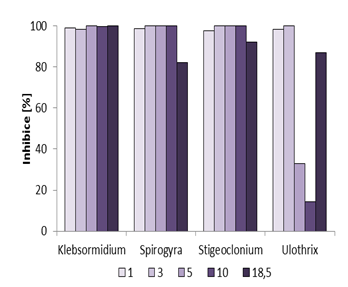
Vláknité řasy mají delší generační cyklus než kokální řasy. Z tohoto hlediska je porovnání účinků nanočástic stříbra složitější. Hodnocení lze provézt pouze na základě stanovení chlorofylu-a na začátku a na konci testu. Na Obr. 1 jsou uvedeny průběhy testů některých vybraných preparátů na řasu Klebsormidium sp. Zvolená délka testu pro zjištění toxicity (zde 96 hodin), resp. hodnoty EC50, je příliš krátká pro řasu Klebsormidium sp. Vláknité řasy mají větší odolnost vůči nanočásticím stříbra v porovnání s chlorokokálními řasami. Průnik nanočástic do nitra buňky nebyl potvrzen ani v případě vláknitých řas. Nelze však vyloučit, že by malé procento částic mohlo proniknout buňkou a napadnout vnitřní struktury buňky. Spíše však dochází k nabalování nanočástic stříbra na povrchu buňky. Tímto způsobem pak brání základním metabolickým funkcím.
Výsledky testování ploch
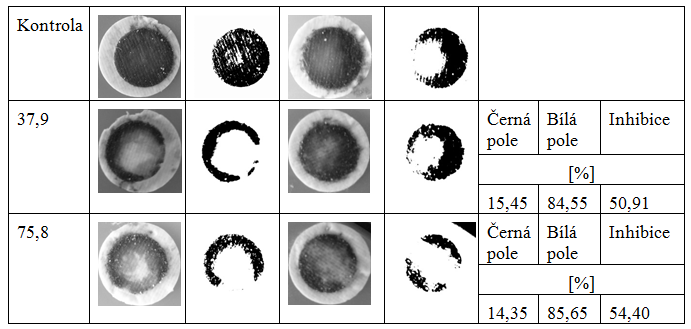
Pro testování řas na povrchu byl vybrán preparát B1. Nasazeny byly pouze koncentrace zahrnující 50 a 100% inhibici.
Závěr
Ze všech připravených preparátů byl nejúčinnější přípravek B1, který obsahoval nanočástice stříbra o velikosti 5 nm. Při porovnání toxicity jednotlivých preparátů na řasu Desmodesmus quadricauda většinou odpovídá jejich velikosti, tedy že se vrůstající velikostí částic klesají toxické účinky. Toto pravidlo však nelze jednoznačně uplatnit pro vláknité řasy. Pro řasu Klebsormidium sp. byl přípravek G1 (galaktózový koloid) mnohem účinnější než ostatní cukerné koloidy, přesto, že obsahuje nanočástice o největší velikosti (70 nm).
Testování povrchů zatím vykazuje dobré výsledky. Touto metodikou by bylo možné testovat povrchy porostlé biofilmy.
Publikace byla vytvořena v rámci projektu č. 217 88 1304
Použitá literatura
- ADÁMKOVÁ P., ŘÍHOVÁ AMBROŽOVÁ J., Říha J. (2012) Využití kovových částic stříbra k potlačování růstu sinic a řas. Vodárenská Biologie 2012, sborník z konference, Říhová Ambrožová J., Veselá J. (ed), Vodní zdroje EKOMONITOR, Chrudim ALI I., (2012) New generation of adsorbents for water treatment. Chem. Rew., 112, 5073 – 5091
- EL-ASSAR HAMMED M., A., SAID M. M., et al. (2013) Using silver nanoparticles coated on activated carbon granules in columns for microbiological pollutants water disinfection in Abu Rawash area, great Cairo, Egypt. Australian Journal of Basic and Applied Sciences, 7(1) 422 - 432
- GARCÍA-CONTRERAS R., ARGUETA-FIGUEROA L., MEJÍA-RUBALCAVA C, et. al. (2011) Perspectives for the use of silver nanoparticles in dental practice. Int Dent J., 61(6), 297-301
- GRIFFIT, R. J.; LUO, J.; GAO, J.; BONZONGO, J. C.; BARBER, D. S. (2008) Effects of particle composition and species on toxicity of metallic nanomaterials in aquatic organism. Environmental Toxicology and Chemistry, 27 (9), 1972–1978.
- GRIFFIT, R. J., HYNDMAN, K., DENSLOW, N. D., BARBER, D. S. (2009) Comparison of Molecular and Histological Changes in Zebrafish Gills Exposed to Metallic Nanoparticles. Toxicological Sciences, 107 (2), 404–415.
- KAEGI, R.; VOEGLIN, A.; SINNET, B.; ZULEEG, S.; et al. (2011) Behavior of Metallic Silver Nanoparticles in a Pilot Wastewater Treatment Plant. Environ. Sci. Technol., 45, 3902–3908. KIM, J. S., et al. (2007) Antimicrobial effects of silver nanoparticles. Nanomedicine: Nanotechnology, Biology and Medicine, 3, 95–101.
- KŘÍŽKOVÁ, S., ADAM, V., KŘÍŽEK, R., et al. (2009) Fytotoxicita stříbrných iontů. Chem. Listy, 103, 559–568.
- KUMAR, R. V.; RAZA, G. (2009) Photocatalytic disinfection of water with Ag–TiO2 nanocrystalline composite. Science and Technology of Ionics , 15, 579–587
- LABAN, G.; NIES, L.; TURCO, R. F.; et al. (2010) The effects of silver nanoparticles on fathead minnow (Pimephales promelas) embryos. Ecotoxicology, (19), 189–195.
- LIGA V. M., BRYANT L. E., et. al. (2011) Virus inactivation by silver doped titanium dioxide nanoparticles for drinking water treatment, Water Reaserch, 45, 535 - 544
- MIAO, A. J.; et al. (2010) The algal toxicity of silver engineered nanoparticles and detoxification by exopolymeric substances. Environmental Pollution, 157, 3034–3041.
- MPENYANA-MONYATSI L., MTHOMBENI N. M. et. al. (2012) Cost – effective filter materials coated with silver nanoparticles for the removal of pathogenic bacteria in groundwater., Int. J. Environ. Res. Public Health, 9, 244 – 271
- MUŇOZ, A. J.; RUIZ, E.; ABRIOEL, H.; GÁLVEZ, A.; et al. (2012) Heavy metal tolerance of microorganisms isolated from wastewaters: Identification and evaluation of its potential for biosorption. Chem. Eng. J. 210, 325–332.
- NAVARRO, E., PICAPPIETRA, F.; et al. (2008) Toxicity of Silver Nanoparticles to Chlamydomonas reinhardtii. Env. Sci. Techn., 8959–8964.
- OUKARROUM, A., POLCHTCHIKOV, S.; et al. (2011) Temperature influence on silver nanoparticles inhibitory effect on photosystem II photochemistry in two green algae, Chlorella vulgaris and Dunaliella tertiolecta., Environ Sci Pollut Res.
- PANÁČEK, A.; KVÍTEK, L.; PRUCEK, R.; et al. (2006) Silver Colloid Nanoparticles: Synthesis, Characterization, and Their Antibacterial Activity. J. Chem. Phys., 110, 16248– 16253.
- PRADEEP T., (2009) Noble metal nanoparticles for water purification: A critical review. Elsevier, 517, 6441 - 6478 REN D., SMITH J. A., (2013) Retention and Transport of silver nanoparticles in a ceramic porous medium used for point-of-use water treatment Environ. Sci. Technol. 47, 3825 – 3832
- SUN, X.; SHENG, Z.; LIU, Y. (2013) Effects of silver nanoparticles on microbial community structure in activated sludge. Sci. Total Environ., 443, 828–835.
- TIWARI K. D., BEHARI J., SEN P., (2008) Application of nanoparticles in waste water treatment. World Applied Sciences Journal, 3 (3), 417 - 433
- WOOD, M. Ch., PLAYLE, R. C., HOGSTRAND, R. C. (1999) Physiology and modelling of mechanisms of silver uptake and toxicity in fish. Environmental Toxicology and Chemistry. 18 (1) 71–83.
- ZHUANG WANG, JINGWEN CHEN.; et al. (2012) Aquatic toxicity of nanosilver colloids to different trophic organisms: Contributions of particles and free silver ion., Environ. Toxicol. Chem., 31 (10), 2408–2413.
Autoři
Ing. Vladimíra Škopová, Vysoká škola chemicko-technologická, Ústav technologie vody a prostředí, Technická 5, 166 28 Praha 6 – Dejvice 166 28



